
50,000,000美元!!!
美国食品药品监督管理局(U.S. FDA)计划于2018财政年度从医疗器械行业收取的使用者费总计为1.8亿美元,相较于2017财政年度的总计1.3亿美元,整整多出了50000000美元。
下图为2013财政年度至2022财政年度医疗器械使用者费的预算,从图中可以看出2018财政年度是一个跨越式的上涨,在后续的5年内还将持续,但是涨幅会趋于平稳。
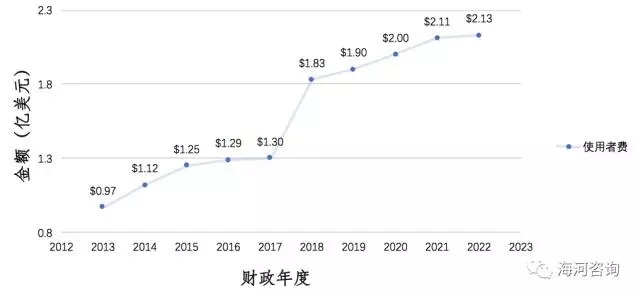
10,000美元!!
2018财政年度医疗器械使用者费的另外一个亮点是510(k)标准审核费,史无前例的达到了10,542美元,相较于2017财政年度的4,690美元,涨幅超过了120%。此外,可能是为了扶持中小企业,510(k)中小企业审核费仍然维持在2,636美元的水平。
新收费项目!
FDA自2018财政年度起,将会对De Novo分类申请收取审核费,De Novo标准审核费为93,017美元(小企业审核费为23,254美元)。De Novo为适用于中低风险的创新医疗器械的申请,它既是一个上市申请,也是一个分类申请,其审核的复杂程度肯定要高于510(k),很奇怪的一点是FDA之前都没有对De Novo审核收取任何费用,所以本次新增为收费项目虽然是意料之外,但也在情理之中,只是FDA被业界诟病阻碍创新估计在所难免。
中小企业资质认定
随着2018财政年度医疗器械使用者费的发布,FDA同时发布了2018财政年度中小企业申请指导原则,与往年相比申请表基本没有改动。任何公司及其附属公司年度销售额小于1亿美元的都可以向FDA申请中小企业资质,享受上市前申请费用的优惠,但是该优惠将不适用于工厂注册年费。
工厂注册年费
2018财政年度医疗器械工厂注册年费为4,375美元,虽然相对于2017财政年度有不少的上涨,但是这主要是因为2017财政年度的工厂注册费原本就低于2016财政年度(海河咨询在2016年8月的推送文章中讨论过原因),而且在其他“亮点”中,这个涨幅就显得有点“波澜不惊”了。
附件
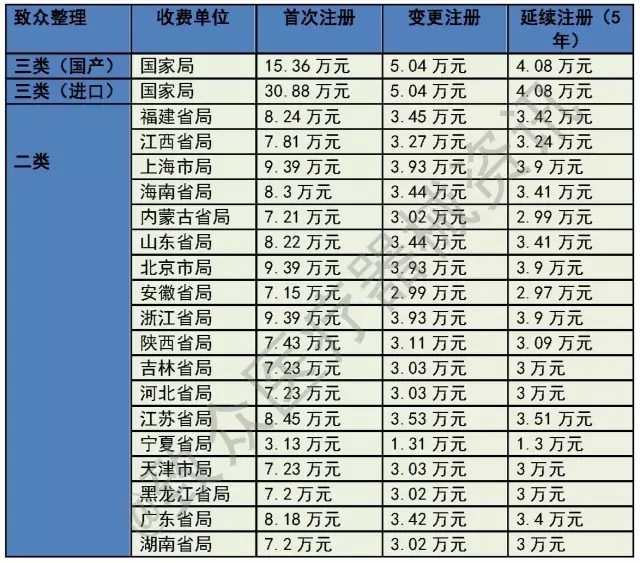
国内各级药监局注册费用汇总表
邮政编码:200052 电话:021-63800152 传真:021-63800151 京ICP备15010734号-10 技术:网至普网站建设